Настанова з якості діагностичної служби медичної установи
Сучасна медицина сліпа без надійного діагнозу. Забезпечення точності, надійності та достовірності відтворення результатів медичних лабораторних досліджень — запорука успіху правильної діагностики пацієнтів. Застосування якісного підходу відповідно до міжнародного стандарту ISO 15189:2012 «Медичні лабораторії — Вимоги до якості та компетентності» може суттєво допомогти досягти цієї мети.
Створення настанови з якості медичної лабораторії, яка контролює всю її документацію, відіграє центральну роль у забезпеченні ефективності системи менеджменту якості. Ця стаття допоможе всім, хто хоче самостійно створити настанову з якості, яка б відповідала критеріям, що визначені вимогами міжнародного стандарту ISO 15189:2012.
Загальні відомості про стандарт ISO 15189:2012
Міжнародний стандарт ISO 15189:2012 заснований на стандартах ISO/IEC 17025:2017 «Загальні вимоги до компетентності випробувальних та калібрувальних лабораторій» та ISO 9001:2015 «Системи менеджменту якості – Вимоги» з метою гармонізації практики акредитації медичних лабораторій. Перша версія цього стандарту вийшла у 2003 році. Чинна версія датується 2012 роком.
Вимоги до акредитації поділені на 2 основні частини:
- частина 1 стосується менеджменту якості;
- частина 2 містить технічні вимоги.
Послуги, які надають лабораторії медичної біології, необхідні для забезпечення якісного догляду за хворими пацієнтами. Отже, вони повинні задовольняти потреби як пацієнтів, так і відповідальних за їхнє лікування лікарів. Лабораторні медичні послуги включають: призначення обстежень, підготовку ідентифікації пацієнтів, збирання, транспортування, зберігання, попередню обробку й аналіз біологічних зразків із наступною інтерпретацією результатів, звітністю та рекомендаціями, забезпечуючи при цьому безпеку та етику медичного персоналу.
Якщо це дозволене національними, регіональними або місцевими законами, бажано, щоб послуги, які надає лабораторія, також включали обстеження пацієнта в рамках консультацій і профілактики, а також діагностику та спостереження за захворюваннями. Також доцільно, щоб кожна лабораторія забезпечувала навчання та наукову підготовку відповідного персоналу.
Незважаючи на те, що стандарт ISO 15189:2012 призначений для ефективного використання лабораторіями медичної біології, він може застосовуватись і в інших секторах діяльності, а також іншими дисциплінами, наприклад, у галузях фізіології, медичної візуалізації та біофізики.
Якщо лабораторія прагне акредитації, вона повинна обрати орган із акредитації, який працює відповідно до ISO/IEC 17011:2017 «Оцінка відповідності — Вимоги до органів з акредитації, які акредитують органи з оцінки відповідності» та який враховує особливі вимоги лабораторій.
Настанова з якості у системі документованої інформації
Настанова з якості — основний документ, який описує систему управління якістю організації. І хоча він не завжди потрібний для деяких систем менеджменту (наприклад, для ISO 9001:2015 «Системи менеджменту якості — Вимоги»), то для стандарту ISO 15189:2012 наявність настанови — обов’язкова.
Так, згідно із п. 4.2.2 стандарту («Вимоги до документації»), документація системи управління якістю лабораторії медичної біології повинна обов’язково включати:
- заяву про політику у сфері якості (п. 4.1.2.3) та цілі з якості (п. 4.1.2.4);
- настанову з якості (п. 4.2.2.2);
- процедури та записи, які необхідні за вимогами стандарту;
- документи та записи (п. 4.13), які визначені лабораторією для забезпечення ефективності планування, виконання та контролю процесів;
- копії відповідних правил, стандартів та інших нормативних документів.
Про настанову з якості, зокрема, йдеться у п. 4.2.2.2 стандарту ISO 15189:2012. Там же дається опис змісту документа, який повинен включати:
- політику у сфері якості (п. 4.1.2.3) або посилання на неї;
- опис галузі застосування системи менеджменту якості;
- представлення структури організації та вищого керівництва лабораторії, її місця у складі медичного закладу;
- опис ролей і відповідальності керівництва лабораторії (включаючи завідувача лабораторії та відповідального з якості) для забезпечення відповідності зі стандартом;
- опис структури та взаємозв’язку документації, що використовується в системі менеджменту якості;
- встановлені для системи менеджменту якості документовані політики та посилання на керівну й технічну діяльність для її підтримки.
Метою настанови з якості лабораторії медичної біології є:
- передача інформації;
- надання доказів дотримання вимог програми акредитації;
- обмін знаннями;
- надання доказу прихильності керівництва до цілей та політики у сфері якості.
При створенні настанови з якості необхідно врахувати такі моменти:
- Це — документ, в якому описується система менеджменту якості установи з використанням низки політик.
- Це — основна документація системи управління якістю, яка повинна містити повний опис.
- Передбачуваний обсяг настанови становить від 30 до 70 сторінок, хоча він може змінюватись залежно від розміру установи, а також від обсягу інформації, яку керівництво закладу вирішує до нього включити.
- Настанова зазвичай включає бізнес-процеси, але не технічні процедури.
- Настанова є дорожньою картою для решти документації лабораторії; це стосується значної кількості документів, таких як процедури (робочі інструкції), записи, форми, діаграми тощо.
- Деякі з цих підтверджуючих документів можуть бути включені до настанови або існувати як її додатки. Однак їх зазвичай створюють окремо від неї. У настанові з якості повинно бути зазначено, де знаходяться ті або інші документи.
- Носій настанови може бути як електронним, так і паперовим.
- Він повинен бути легкодоступним.
- Зазвичай настанова постійно оновлюється та перевіряється менеджером з якості.
- Дуже важливо, щоб весь персонал знав і розумів зміст настанови та інших документів, які у ній згадуються.
Структура та зміст настанови з якості
Формат, структура та зміст настанови з якості залишаються на розсуд кожного медичного закладу. Настанова складається відповідно до розміру (штат персоналу, наявність контрольованих активів) і складності закладу (організаційна структура, процеси тощо). Оскільки типи закладів дуже відрізняються, немає стандартного зразка настанови з якості. Тому слід організувати настанову так, як це зручно керівництву установи, розбивши її на розумні частини. При цьому слід переконатися, що вона містить щонайменше наступне:
- вступ (огляд настанови);
- опис організації;
- заяву про політику у сфері якості;
- опис елементів системи управління якістю;
- зміст настанови;
- посилання на інші документи;
- правильну ідентифікацію документів.
Під час розробки змісту настанови з якості слід взяти до уваги, що система менеджменту якості повинна охоплювати всі процеси управління, що пов’язані з забезпеченням якості.
Перелік необхідних елементів настанови також наводиться у вимогах II.A.2 програми Інституту управління якістю сфери охорони здоров’я (IQMH, Canada). Відповідно до цієї програми система менеджменту якості повинна включати всі пов’язані із забезпеченням якості дії та процеси, зокрема:
- організацію;
- персонал;
- обладнання;
- постачання та запаси (включаючи кваліфікацію та моніторинг постачальників);
- управління технологічним процесом;
- документи та записи;
- управління інформацією;
- розслідування невідповідностей;
- оцінку (включаючи використання показників якості, внутрішнього аудиту й аналізу з боку вищого керівництва);
- постійне вдосконалення;
- клієнторієнтований сервіс;
- зручність і безпеку.
І все ж таки, яку структуру настанови з якості можна було б застосувати? Давайте розглянемо деякі варіанти.
Перший варіант: дотримуватись структури стандарту ISO 15189:2012
У таблиці 1 представлений підхід, який заснований на назвах, що містяться в структурі стандарту ISO 15189:2012. При такому підході короткий виклад стандарту ISO 15189:2012 стає змістом настанови з якості; навіть метод нумерації залишається тим самим. Цей метод має ту перевагу, що спрощує завдання визначення того, наскільки виконані всі вимоги ISO 15189:2012. Проте слід додати частини, що описують систему інформації та здійснення біологічних аналізів поза межами лабораторії.
Другий варіант: дотримуватися рекомендацій Інституту клінічних і лабораторних стандартів (CLSI)
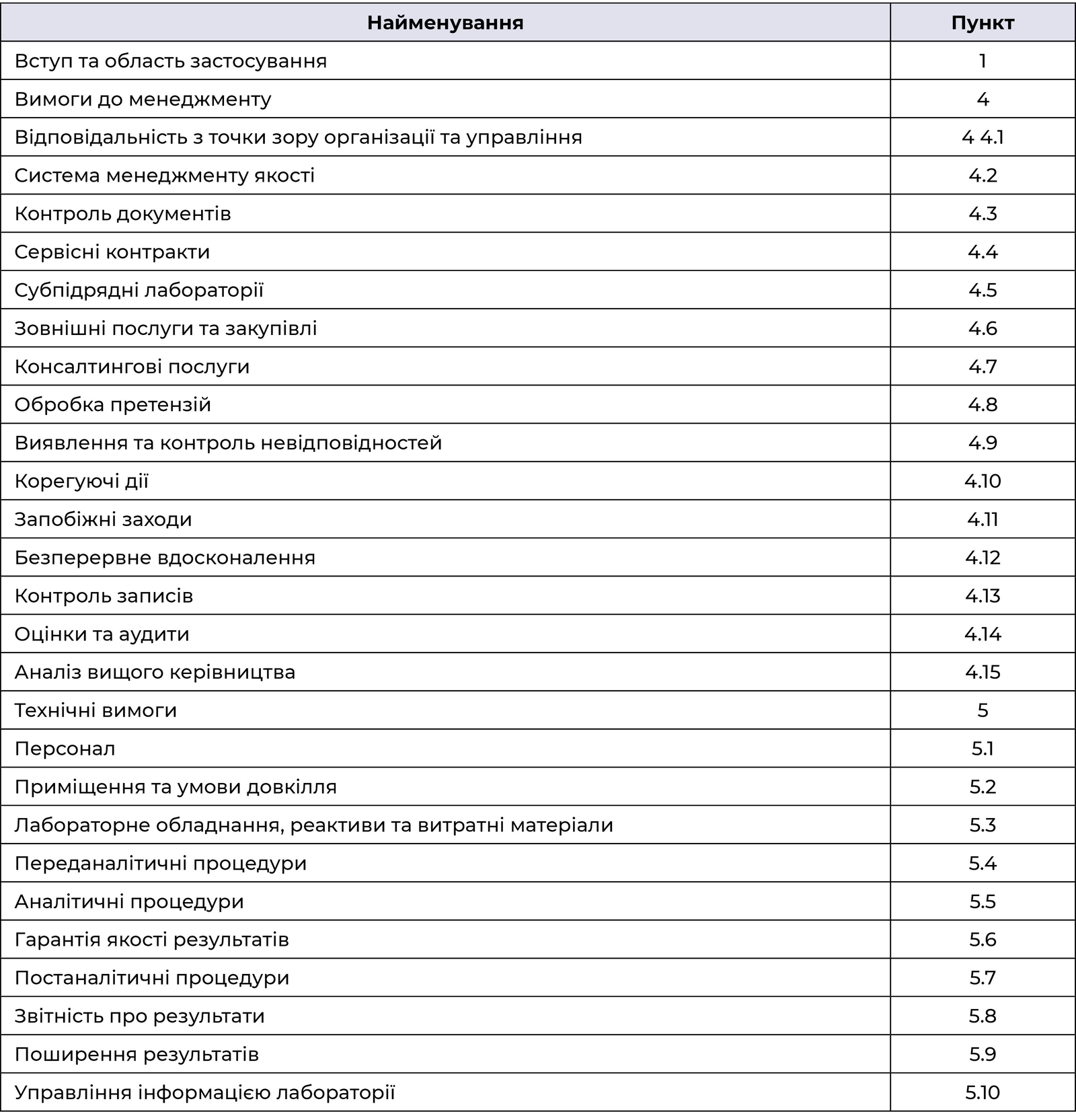
Інша ефективна модель полягає у використанні дванадцяти основних принципів системи якості, що описані Інститутом клінічних лабораторних стандартів (CLSI, США). У таблиці 2 представлений зміст, який розроблений із використанням цього підходу. Перелічені основні види діяльності та процеси засновані на документі CLSI QMS01-A4 «Система управління якістю: модель лабораторних послуг». Назви в цьому списку можна легко взяти за основу настанови з якості, додавши вступ, глосарій, загальну інформацію, опис системи менеджменту якості та історію змін.
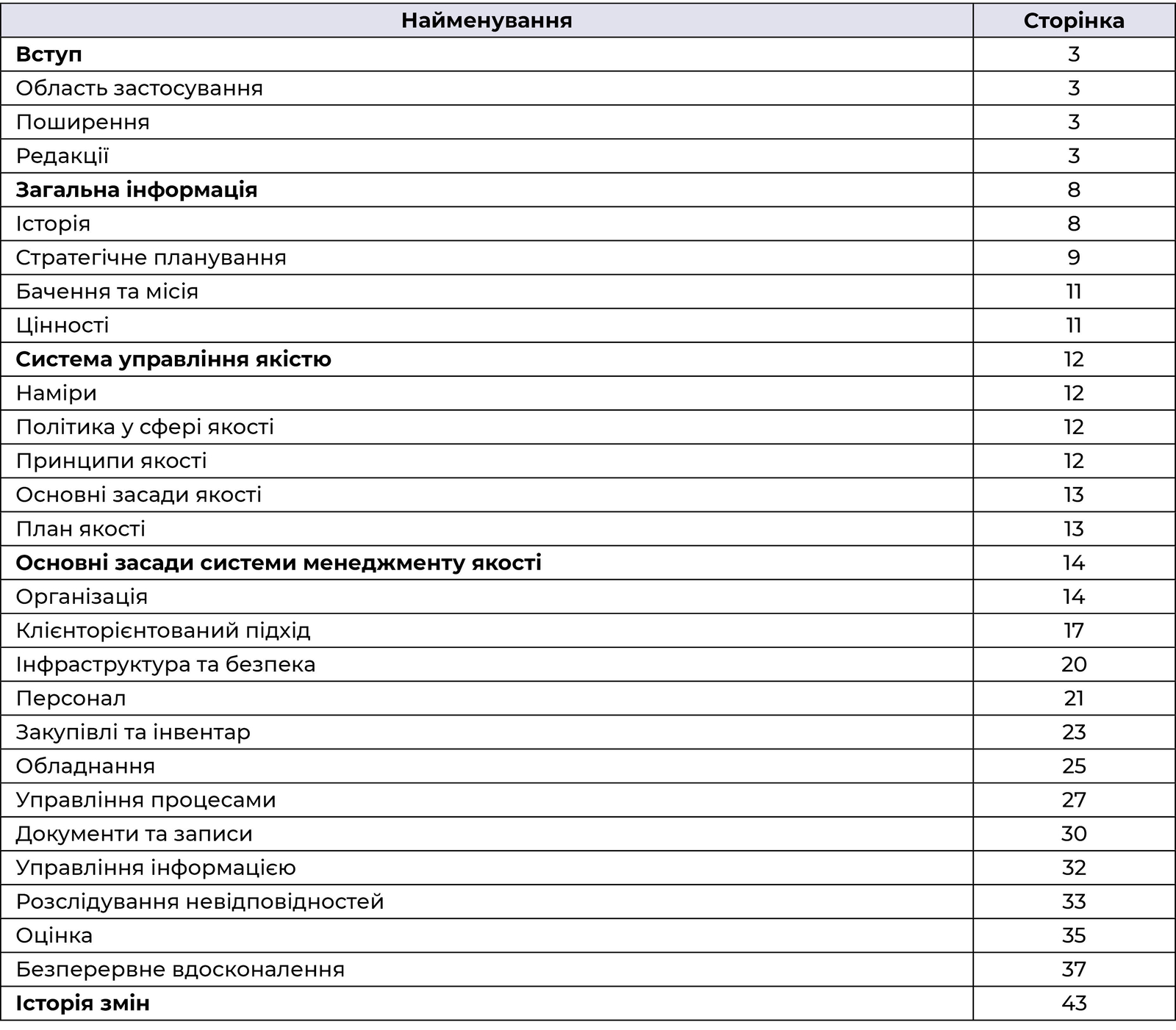
Третій варіант: дотримуватись структури вимог програми акредитації Інституту менеджменту якості у сфері охорони здоров’я (IQMH, Canada)
Таблиця 3 — приклад змісту, структура якого відповідає вимогам програми IQMH. У цьому прикладі, як і в другому варіанті, вимоги програми перетворюються з набору вимог до зобов’язань медичної установи виконувати ці вимоги. Використання такої структури спростить читання настанови для користувача та допоможе гарантувати, що нічого не буде втрачено.
Четвертий варіант: дотримуватись структури стандарту ISO 9001:2015
Як уже згадувалося вище, стандарт ISO 9001:2015 не вимагає настанови з якості, але багато підприємств медичної галузі продовжують створювати її відповідно до структури вимог ISO 9001:2015. Цей варіант відповідає вимогам IQMH та принципам ISO 9000:2015 «Системи менеджменту якості — основи та словник». У цій моделі стандарт ISO трансформується з набору вимог до зобов’язань медичної установи виконувати ці вимоги у формі коротких і точних формулювань. Настанова з якості відповідає стандарту ISO, а структура нумерації така сама, як і в ISO 9001:2015.
П’ятий варіант: створити власну структуру настанови
Медична установа (її підрозділ як лабораторія, діагностична служба) може вирішити створити власну структуру настанови. У цьому випадку слід пам’ятати, що настанова з якості повинна охоплювати всі ключові елементи вимог програми акредитації.
Вступ настанови з якості
У настанові з якості короткий вступ повинен містити огляд настанови з якості медичної установи або окремої її служби.
У «Вступі» необхідно розглянути можливість включення наступної інформації:
- ПІБ особи, яка перевірила та затвердила настанову з якості;
- версію та дату публікації поточної версії;
- обсяг та загальні правила використання настанови;
- інформацію про режим редагування настанови;
- інформацію про поширення як «для внутрішнього», так і «для зовнішнього» користування;
- інформацію про медичний заклад:
- назву, адресу, номер телефону, адресу електронної пошти тощо;
- обсяг запропонованих аналізів біологічних зразків;
- історію медичного закладу;
- бачення, місію, цінності;
- терміни або глосарій;
- зміст настанови.
Заява про прихильність політиці з якості
Заява вищого керівництва медичної лабораторії про політику у сфері якості спрямована на визначення намірів і напрямків розвитку системи менеджменту якості. Така заява підтверджує, що вище керівництво власним прикладом наочно демонструє всім зацікавленим особам свою відданість якості. Ця заява дуже важлива, тому що лідери формують культуру якості, а їхня прихильність — ключ до успіху.
Така заява про політику якості повинна щонайменше включати:
- відданість діагностичної служби відповідати сучасній передовій професійній практиці, якості аналізу біологічних зразків, дотриманню системи управління якістю та її постійному вдосконаленню;
- орієнтацію на своїх клієнтів;
- забезпечення основ для встановлення цілей у сфері якості;
- відповідність цілям медичного закладу;
- доведення до відома всього персоналу та інших зацікавлених осіб;
- забезпечення перегляду політики та її актуалізації.
Контроль документів і записів
Настанова з якості, як основний документ, впроваджує систему управління документами та записами. Ця система повинна бути описана в заяві про політику та підтримуватись відповідними процесами і процедурами.
Основні документи системи управління якістю повинні бути доступні у всіх місцях, де здійснюється діяльність лабораторії медичної біології, що необхідне для ефективного функціонування всієї діагностичної служби.
Всі документи, що розповсюджуються серед працівників в межах системи управління якістю, повинні бути перевірені та затверджені для використання керівником або уповноваженою на це особою (менеджером із якості).
Документи слід переглядати та періодично оновлювати, щоб гарантувати, що вони актуальні та відповідають своєму призначенню.
Усі внесені до документів зміни повинні бути ідентифіковані.
Список (або реєстр документів) повинен вестись із зазначенням поточних змін.
Усі документи, що належать до системи управління якістю, повинні містити:
- назву;
- унікальний ідентифікатор кожної сторінки;
- дату поточної версії та/або номер версії;
- номери сторінок із зазначенням загальної кількості сторінок;
- орган публікації.
Для управління системою документованої інформації повинні бути затверджені відповідні процедури управління документами, щоб гарантувати, що застарілі документи видаляють і що поточна версія відповідних документів може активно використовуватися.
Термін зберігання застарілих документів повинен бути визначений.
Збережені або заархівовані застарілі документи повинні бути визначені як застарілі, щоб запобігти їхньому ненавмисному використанню.
Під час оформлення документів системи управління якістю, зокрема настанови з якості, чимале значення відіграють верхні та нижні колонтитули.
На рисунках 1–4 показані приклади верхніх і нижніх колонтитулів, які відповідають вимогам ідентифікації документів. Будь-який із цих верхніх і нижніх колонтитулів можна адаптувати до настанови з якості та всіх пов’язаних документів у системі менеджменту якості. Зверніть увагу, що нумерація сторінок може бути безперервною або частковою.


Під час використання настанови з якості необхідно періодично перевіряти, що вона:
- актуальна;
- прочитана всім персоналом;
- щорічно переглядається найвищим керівництвом медичного закладу.
Рекомендується включити в настанову з якості сторінку із «записами змін». Її доцільно розмістити перед вступом до настанови. Також можна включити історію змін кожної політики у стандартний верхній або нижній колонтитул.
Якщо настанова з якості переважно є електронним документом, у якому неконтрольовані паперові копії можуть бути роздруковані для тимчасового користування, слід подумати про додавання нижнього колонтитулу на кожну сторінку, що роздруковується. Будь-який документ, представлений у паперовій копії, перед використанням необхідно звіряти з версією файлу, збереженого на сервері.
Персонал повинен мати доступ тільки до останніх версій будь-якого документа. Якщо працівникам необхідно мати паперові копії для повсякденної роботи, керівництво повинне надати їм контрольовані копії. Якщо вони розміщені на внутрішньому сайті та використовуються співробітниками, вони повинні бути оновлені. Друковану копію необхідно періодично перевіряти.
Аналіз і перегляд настанови з якості
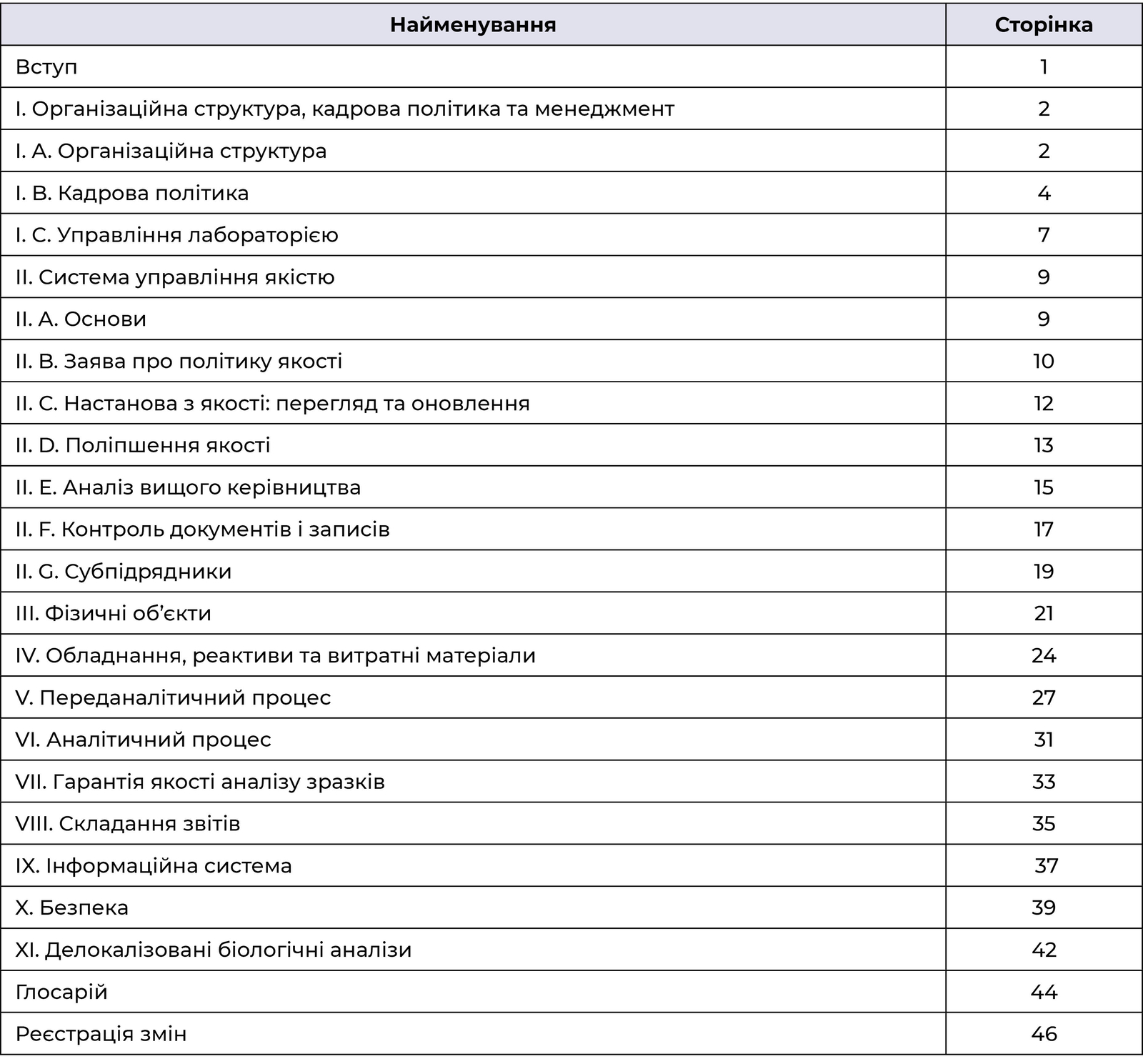
Медична установа (її служба з діагностики або медична лабораторія) повин-на представляти свою настанову з якості перед кожним візитом зовнішніх аудиторів.
Таблиця 4 може бути корисною для самооцінки настанови з якості. Перелік політик, включених до форми, включає ті з них, які зовнішні аудитори очікують побачити в настанові з якості. Установам рекомендується включати інформацію, зазначену в їхніх настановах з якості, щоб самооцінка була ефективною та прискорила проходження аудиту. Однак той факт, що політика не включена до настанови з якості, не буде недоліком, якщо інформація задокументована в іншому місці. За кожним критерієм, зазначеним у Таблиці 4, медична служба повинна вказати номер сторінки настанови з якості, що містить цю інформацію, або вказати, де аудитори можуть знайти документацію, що належить до них.